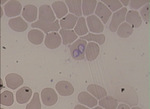
Babeszjoza psów jest pasożytniczą chorobą powodowaną przez przenoszone przez kleszcze pierwotniaki z rodzaju Babesia (1). U psów w Polsce dotychczas stwierdzono występowanie jedynie gatunku Babesia canis (ryc. 1) (2, 3). Ponadto chorobę tę mogą wywoływać również niewystępujące w naszym kraju gatunki, takie jak B. vogeli, B. rossi, B. conradae oraz B. gibsoni (1, 4). Żywicielem ostatecznym pierwotniaka są kleszcze należące do rodziny Ixodidae. Spośród wielu gatunków kleszczy przenoszących pierwotniaki z rodzaju Babesia u psów, w Polsce dotychczas stwierdzono występowanie jedynie kleszcza łąkowego – Dermacentor reticulatus, który jest żywicielem B. canis. Ponadto sporadycznie zawlekany jest do Polski kleszcz Rhipicephalus sanguineus, będący wektorem B. gibsoni i B. vogeli (1, 5, 6).
Summary
Pancreatitis – severe complication of canine babesiosis
Canine babesiosis is a tick-borne protozoan disease. Pancreatitis is one of most severe complications of canine babesiosis. This complication has been described in dogs infected with Babesia rossi and Babesia canis in South Africa and Hungary. The diagnosis of pancreatitis is difficult and prognosis during the course of babesiosis is poor. This article describes the pathogenesis, diagnosis and treatment of pancreatitis in dogs infected with protozoans of the genus Babesia.
Key words: canine babesiosis, complications, pathogenesis, pancreatitis
Żywicielem pośrednim pierwotniaków z rodzaju Babesia są ssaki, w tym psy, i sporadycznie ptaki (7). Cykl rozwojowy pasożyta składa się z trzech etapów: merogonii, gamogonii i sporogonii. Pierwszy z nich ma miejsce w organizmie żywiciela pośredniego. Sporozoity wprowadzone wraz ze śliną kleszcza zasiedlają czerwone krwinki, w których przekształcają się w trofozoity. Trofozoity dzielą się na potomne komórki, nazywane merozoitami. Merozoity opuszczają erytrocyty, doprowadzając do ich rozpadu, po czym zasiedlają następne erytrocyty, przekształcając się ponownie w trofozoity. Cykli trofozoit–merozoit może być wiele, a ta część cyklu rozwojowego nosi właśnie nazwę merogonii. Kleszcze zarażają się, pijąc krew żywiciela pośredniego zawierającą erytrocyty z merozoitami. Dalsze etapy cyklu rozwojowego mają miejsce w organizmie kleszcza (7).
Babeszjoza psów
Przebieg choroby u psów jest zróżnicowany i zależny z jednej strony od gatunku pasożyta, z drugiej zaś od odpowiedzi immunologicznej żywiciela. Najcięższy przebieg choroby obserwowano u psów w RPA zarażonych B. rossi, natomiast najłagodniejszą postać choroby powoduje inwazja wywołana przez B. vogeli (1). Choroba spowodowana przez B. canis ma przebieg od umiarkowanego do ciężkiego, stwierdzano jednak również przypadki bezobjawowego nosicielstwa (1, 8). Objawy babeszjozy u psów są mało swoiste. Obserwuje się brak apetytu, apatię, wymioty, biegunkę, hemoglobinurię, skąpomocz lub bezmocz oraz sporadycznie objawy neurologiczne. W badaniu klinicznym stwierdzano gorączkę, przyspieszenie tętna i oddechów, odwodnienie, zażółcenie lub bladość błon śluzowych oraz ból brzucha. Choroba zbyt późno rozpoznana bądź nieleczona może skończyć się śmiercią (1).
W badaniach laboratoryjnych stwierdzano małopłytkowość, niedokrwistość oraz neutropenię z przesunięciem obrazu w lewo. Małopłytkowości oraz niedokrwistości może towarzyszyć wzrost średniej objętości krwinek czerwonych oraz płytek. Ponadto w przypadku krwinek czerwonych opisywano anizocytozę, polichromazję oraz poikilocytozę (9). W badaniach biochemicznych surowicy obserwowano podwyższone stężenie mocznika, kreatyniny, bilirubiny, hormonu adrenokortykotropowego i kortyzolu. Ponadto stwierdzano obniżenie stężenia glukozy, albumin oraz całkowitej i wolnej czterojodotyroniny. W badaniach określających aktywność enzymów obserwowano wzrost aktywności fosfatazy zasadowej, transaminazy alaninowej i asparaginianowej, γ-glutamylotransferazy oraz amylazy i lipazy (10, 11, 12, 13). Wzrost aktywności amylazy i lipazy w przebiegu babeszjozy psów może wynikać z obniżonej filtracji nerkowej bądź też z zapalenia trzustki. Należy również pamiętać, że niektóre leki (np. glikokortykosteroidy) mogą powodować podwyższenie aktywności tych enzymów w surowicy. Ponadto możliwy jest wzrost aktywności tych enzymów w przypadku chorób jelit oraz wątroby (14, 15).
Zapalenie trzustki u psów
Zapalenie trzustki u psów może być ostre lub przewlekle, aczkolwiek w przebiegu tych dwóch typów zapaleń różnica polega przede wszystkim na zmianach histopatologicznych i nie zawsze musi pokrywać się z przebiegiem klinicznym choroby. Przewlekłe zapalenie trzustki może mieć w niektórych przypadkach przebieg łagodniejszy, jednakże ostateczne zróżnicowanie zapaleń ostrych i przewlekłych możliwe jest dopiero na podstawie badań histopatologicznych (16, 17). W ostrych zapaleniach trzustki często dominują zmiany martwicowe. Z kolei w przewlekłym zapaleniu w badaniach histopatologicznych stwierdza się przede wszystkim zwłóknienie oraz zanik miąższu (18).
Przyczynami zarówno ostrych, jak i przewlekłych zapaleń trzustki u psów mogą być: niedrożności przewodów trzustkowych, bezpośrednie uszkodzenia komórek pęcherzykowych trzustki oraz zaburzenia enzymatyczne powodujące nadmierną przedwczesną aktywację trypsynogenu do trypsyny jeszcze w obrębie trzustki. Te ostatnie prowadzą do uwalniania aktywnego enzymu trawiennego do miąższu narządu, czego efektem jest samotrawienie trzustki i w konsekwencji jej martwica. Ponadto do uszkodzenia trzustki może dochodzić w wyniku urazów mechanicznych powodujących uwolnienie enzymów trzustkowych do miąższu narządu. Mechanizm prowadzący do uszkodzenia tego narządu u psów nie jest jednak do końca poznany. Wiadomo na przykład, że u psów może dojść do rozwoju zapalenia trzustki w konsekwencji zjedzenia obfitego tłustego posiłku (18). Ponadto stwierdzono występowanie predylekcji związanych z rasą, płcią i otyłością. Zapalenia trzustki obserwowano częściej u sznaucerów miniaturowych, otyłych psów oraz wysterylizowanych suk. Nie jest jednak jasne, czy predyspozycje rasowe są związane z uwarunkowaniami genetycznymi i dziedzicznym zapaleniem trzustki, którego występowanie udowodniono u człowieka (16, 17, 18).
Patogeneza i objawy zapalenia trzustki u psów
Główną rolę w rozwoju zapalenia trzustki odgrywa trypsyna, która jest uwalniana do miąższu narządu w wyniku nadmiernej i przedwczesnej aktywacji trypsynogenu wewnątrz komórek pęcherzykowych. Dzieje się tak na skutek nieprawidłowego łączenia się ziarnistości zawierających trypsynogen z lizosomami, co prowadzi do powstawania wakuoli, w których obniżone pH lub lizosomalna hydroliza proenzymów trypsyny powodują ich aktywację do enzymu. Zostaje wtedy przełamana bariera molekularnych inhibitorów trypsyny, co skutkuje strawieniem komórek pęcherzykowych i uwolnieniem enzymu do miąższu narządu (16, 17). Konsekwencją uwolnienia trypsyny jest aktywacja proenzymów do aktywnych enzymów, takich jak elastaza i fosfolipaza A2. Enzymy te prowadzą do strawienia miąższu trzustki oraz otaczającego ją tłuszczu. Ponadto aktywacji ulega również prekalikreina, prowadząc do aktywacji układu dopełniacza oraz kaskady krzepnięcia krwi. Skutkuje to pojawianiem się krwawień oraz zakrzepów w obrębie narządu i naciekiem komórek zapalnych. W rozwoju uszkodzenia trzustki istotną rolę odgrywają też mediatory procesu zapalnego, takie jak interleukiny prozapalne, TNF-α, tlenek azotu oraz wolne rodniki tlenowe, uwalniane przez komórki nacieku zapalnego. Zapalenie trzustki oraz martwica otaczającego ją tłuszczu mogą prowadzić w konsekwencji do rozwoju zapalenia otrzewnej (16, 17, 18).
Nasilenie objawów zapalenia trzustki u psów jest zależne od stopnia uszkodzenia samego narządu oraz od występowania równocześnie uszkodzenia innych narządów bądź powikłań. Zapalenie trzustki może objawiać się łagodnym bólem brzucha lub też zespołem ostrego brzucha. U chorych psów obserwowano wymioty i biegunkę prowadzące do odwodnienia, ból brzucha, brak apetytu oraz gorączkę. Ponadto w przebiegu zapalenia trzustki u psów obserwowano zespół rozsianego krzepnięcia wewnątrznaczyniowego, zapalenie tkanki podskórnej w wyniku znacznego wzrostu aktywności lipazy w surowicy oraz wstrząs (16, 17, 19).
Zapalenie trzustki jako powikłanie babeszjozy
Zapalenie trzustki może być jednym z powikłań babeszjozy. Po raz pierwszy potwierdzone w badaniach histopatologicznych zapalenie trzustki stwierdzono u psów zarażonych B. rossi w RPA w roku 2000 (20). Kolejne przypadki zapalenia trzustki u psów w przebiegu babeszjozy rozpoznano na Węgrzech (13). Jednakże na Węgrzech psy zarażone były B. canis – tym samym gatunkiem, który występuje w Polsce. W badaniach retrospektywnych Máthé i wsp. (13) stwierdzili, że powikłana babeszjoza, czyli taka, w której przebiegu rozpoznano zespół uogólnionej reakcji zapalnej oraz zespół niewydolności wielonarządowej, występowała u 49,2% zarażonych psów. Natomiast u 33% spośród psów z powikłaną babeszjozą rozpoznano zapalenie trzustki. Warto wspomnieć, że powikłaną postać babeszjozy obecnie klasyfikuje się jako ciężką posocznicę pierwotniaczą, a prawdopodobieństwo jej wystąpienia w przebiegu tej choroby wzrasta wraz z wiekiem (10, 13, 21, 22, 23, 24). Máthé i wsp. (13) stwierdzili również, że zapalenie trzustki nigdy nie występowało jako jedyne powikłanie choroby, lecz towarzyszyła mu na ogół ostra niewydolność nerek lub uszkodzenie wątroby. Podobne wyniki uzyskali w swoich badaniach Möhr i wsp. (20). Stwierdzili oni, że w większości przypadków zapaleń trzustki u psów zarażonych B. rossi występowały również uszkodzenia innych narządów.
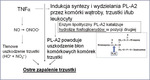
Mechanizm prowadzący do rozwoju zapalenia trzustki u psów zarażonych pierwotniakami z rodzaju Babesia nie jest do końca poznany. Möhr i wsp. (20) sugerują, że niedokrwienie i niedotlenienie trzustki może być jedną z przyczyn uszkodzenia tego narządu. Wydaje się jednak prawdopodobne, że również nadprodukcja prozapalnych cytokin oraz reaktywnych form tlenu może odgrywać rolę w uszkodzeniu trzustki, podobnie jak ma to miejsce w uszkodzeniu trzustki u ludzi (25, 26). Obecnie istnieje pogląd, że ciężki przebieg babeszjozy, podobnie jak w przypadku malarii u ludzi, spowodowany jest nadprodukcją cytokin prozapalnych, takich jak INFγ i TNFα (24, 27). Wytwarzany przez aktywowane makrofagi w nadmiarze TNFα prowadzi do aktywacji enzymu indukowalnej syntazy tlenku azotu, który syntetyzuje tlenek azotu z L-argininy przy udziale NADPH i cząsteczki tlenu. Powstający tlenek azotu w reakcji z anionorodnikiem ponadtlenkowym, którego źródłem może być reakcja utleniania hemoglobiny uwolnionej z uszkodzonych wewnątrznaczyniowo erytrocytów, prowadzi do powstawania nadtlenoazotynu, który z kolei w reakcji protonacji tworzy kwas nadtlenoazotawy, będący źródłem wolnych rodników, takich jak rodnik hydroksylowy i dwutlenek azotu, biorących udział w tlenowym uszkodzeniu błon komórkowych komórek trzustki (26, 27, 28, 29).
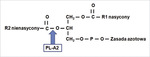
Z drugiej strony wiadomo również, że w uszkodzeniu trzustki istotną rolę odgrywa enzym lipolityczny fosfolipaza A2, który katalizuje hydrolizę trójglicerydów w pozycji drugiej (ryc. 2). Wydaje się prawdopodobne, że podobnie jak ma to miejsce u ludzi zarażonych zarodźcami z rodzaju Plasmodium, produkowany i wydzielany w nadmiarze TNFα indukuje syntezę i wydzielanie fosfolipazy A2 przez komórki wątroby, trzustki oraz ewentualnie leukocyty, prowadząc w ten sposób do uszkodzenia błon komórkowych trzustki (30, 31). Możliwe jest też, że do uszkodzenia i w konsekwencji zapalenia trzustki w przebiegu babeszjozy psów dochodzi w wyniku wszystkich proponowanych mechanizmów. Schemat prawdopodobnych mechanizmów uszkodzenia trzustki u psów zarażonych pierwotniakami z rodzaju Babesia przedstawiono na ryc. 3.
W przebiegu zapalenia trzustki u psów zarażonych B. rossi stwierdzono ból brzucha, żółtaczkę, wymioty, biegunkę oraz smolisty kał (24). Z kolei u psów zarażonych B. canis nie stwierdzano w badaniu klinicznym bolesności brzucha, występowały natomiast wymioty oraz hiperglikemia. Liczba leukocytów u tych psów pozostawała w granicach norm fizjologicznych. Nie oznacza to jednak, że przebieg samej babeszjozy u psów zarażonych B. canis był łagodny, gdyż większość zwierząt, u których doszło do rozwoju zapalenia trzustki, nie przeżyła (13).