Postępowanie żywieniowe w przypadku chłonkopiersia – opis przypadku
Laura Gaylord, Donna Raditic
Chłonkopiersie definiuje się jako nagromadzenie zmodyfikowanego płynu limfatycznego w jamie opłucnej. Prawidłowe trawienie i wchłanianie tłuszczu z przewodu pokarmowego powoduje, że triglicerydy z żywności są w komórkach błony śluzowej jelita czczego pakowane w chylomikrony, które dostają się do układu limfatycznego. Chłonka z limfatycznych naczyń lędźwiowych i krezkowych przepływa do zbiornika chłonki, a następnie do przewodu piersiowego, gdzie wchodzi do krążenia żylnego. W przypadku przerwania tej drogi lub wzrostu ciśnienia w układzie limfatycznym może dojść do chłonkopiersia w wyniku wycieku chłonki do przestrzeni opłucnowej.
Do głównych przyczyn chłonkopiersia należą: ucisk przewodu piersiowego, nowotwór, grasiczak, choroba grzybicza lub skręt płata płuca. Chłonkopiersie może być również spowodowane zwiększonym układowym ciśnieniem żylnym wynikającym z prawostronnej niewydolności serca, robaczycy serca, płynu w worku osierdziowym, kardiomiopatii, dysplazji zastawki trójdzielnej, zaburzeń zatorowo-zakrzepowych.1,2 Chociaż rzadko, chłonkopiersie może wynikać z przepukliny przeponowej, operacji klatki piersiowej, urazu lub silnego kaszlu albo wymiotów. W wielu przypadkach dokładna przyczyna chłonkopiersia nie jest znana i dlatego jest ono określane jako idiopatyczne.2 Objawy kliniczne chłonkopiersia odnoszą się do choroby jamy opłucnej i mogą być ostre lub przewlekłe. Pacjenci dotknięci chorobą mają przyspieszony oddech (tachypnea) albo więcej łagodnych objawów (na przykład senność, brak łaknienia, kaszel, nietolerancja wysiłku). Ponieważ chłonka zawiera wodę, elektrolity, lipidy, białka i witaminy rozpuszczalne w tłuszczach, drenaż i usunięcie chłonki z przestrzeni opłucnej może spowodować odwodnienie i zaburzenia równowagi elektrolitowej. Przewlekłe i nawracające chłonkopiersie może również powodować zaciskające zapalenie opłucnej, co pogarsza rokowanie. Zalecane leczenie chłonkopiersia obejmuje interwencję żywieniową, farmakologiczną i/lub chirurgiczną.1 Niniejszy opis przypadku przedstawia podejście żywieniowe do leczenia chłonkopiersia, które zostało zainicjowane w celu ustabilizowania pacjenta do ewentualnego leczenia chirurgicznego.
Historia i opis pacjenta
Pacjentem był pięcioletni kastrowany pies rasy goldendoodle o masie 31 kg, z oceną kondycji ciała 4/9 (Purina Body Condition System) i prawidłową kondycją mięśni (ryc. 1). U psa od sześciu tygodni występowała postępująca hiporeksja (zaburzenia łaknienia) z okresową sennością i napadami wymiotów oraz miękkim kałem (ocena kału od 4 do 5/9, Purina Fecal Scoring Chart). Miał również historię zapalenia przewodu słuchowego zewnętrznego, podejrzenie atopii i przewlekłej enteropatii, które były leczone lekiem miejscowym (steroid/lek przeciwgrzybiczy/antybiotyk), iniekcjami lokivetmabu (Cytopoint) i hydrolizowaną weterynaryjną dietą terapeutyczną (Hill’s Prescription Diet z/d) podawaną w ilości 1,5 filiżanki dwa razy dziennie (1062 kcal/dzień). Pacjent otrzymywał przez cały rok środki zapobiegające inwazji nicieni sercowych oraz pcheł/kleszczy, a wszystkie szczepienia były aktualne.
Wstępna ocena pacjenta
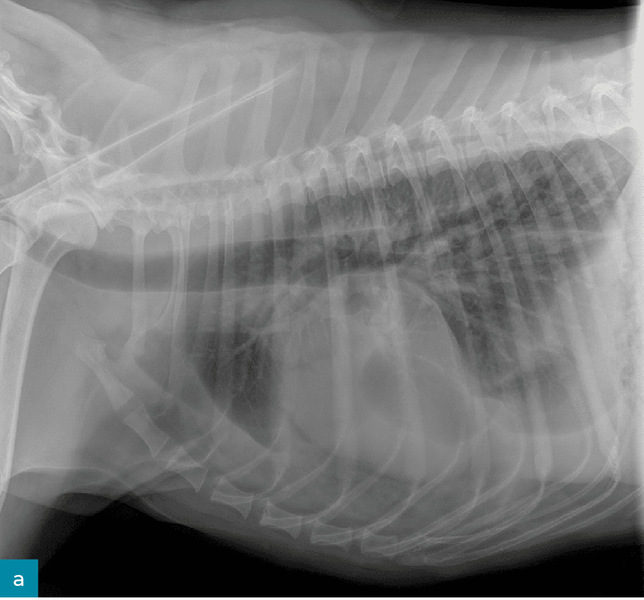
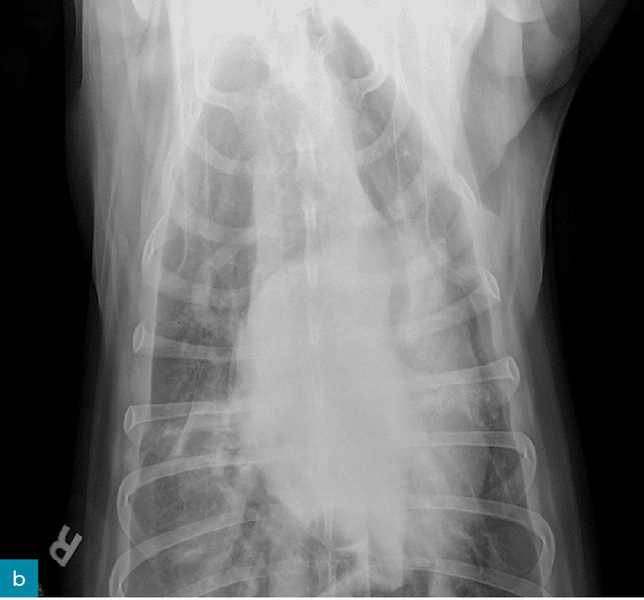
Lekarz weterynarii podstawowej opieki zdrowotnej poinformował, że badanie kliniczne pacjenta było w normie: temperatura wynosiła 38,2°C, częstość pracy serca 90 uderzeń/min, a częstość oddechów 35/min przy normalnym wysiłku. Odnotowano utratę masy ciała o 2 kg – podczas corocznego badania sześć miesięcy wcześniej wynosiła ona 33 kg. Wykonano przesiewowe badanie rentgenowskie jamy brzusznej oraz klatki piersiowej i zidentyfikowano płyn w przestrzeni opłucnowej (ryc. 2). Pacjent został skierowany do placówki specjalistycznej/ratunkowej w celu przeprowadzenia dodatkowej diagnostyki.
W ośrodku ratunkowym pacjent był ożywiony, czujny i reagował na bodźce. Stwierdzono szmer skurczowy serca stopnia 2/6. Radiogramy klatki piersiowej potwierdziły płyn w jamie opłucnej i wykazały łagodną niedodmę doogonowych pól płucnych. Podczas nakłucia klatki piersiowej usunięto około 3 ml białego, mlecznego płynu z lewej doczaszkowej części klatki piersiowej i około 20 ml z prawej części klatki piersiowej. Rodzaje płynu gromadzącego się w przestrzeni opłucnej obejmują przesięk, zmodyfikowany przesięk, wysięk oraz wysięk limfatyczny. Biorąc pod uwagę wygląd płynu, podejrzewano wysięk limfatyczny. Ostateczne rozpoznanie chłonkopiersia opiera się na wykryciu w płynie stężenia triglicerydów wyższego niż w surowicy. Płyn został przesłany wraz z krwią i moczem do badań diagnostycznych.
Badania diagnostyczne i wyniki
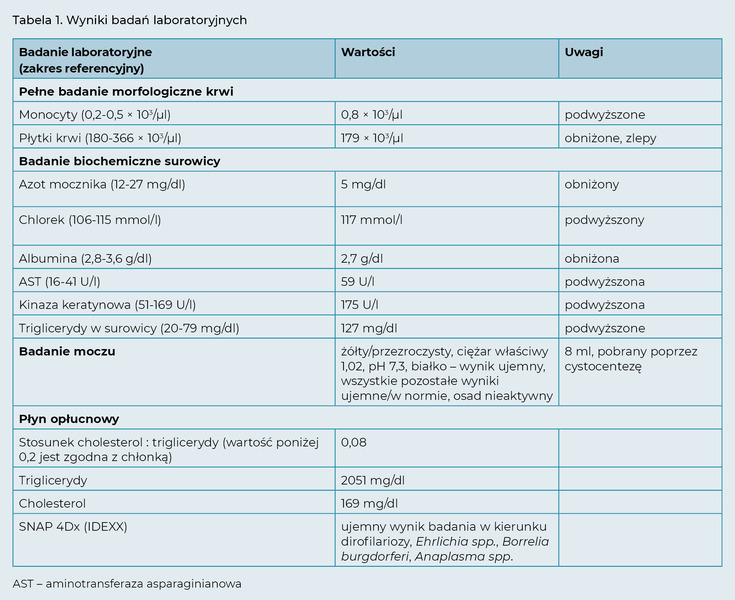
Wyniki badań laboratoryjnych krwi, moczu i płynu opłucnowego (nie podano stężenia białka) przedstawiono w tabeli 1. Bezpośrednie rozmazy płynu opłucnowego zawierały niewielką liczbę komórek jądrzastych i erytrocytów na różowym tle. Komórki jądrzaste były głównie limfocytami (60-65%, przede wszystkim małe, kilka średnich i dużych) z umiarkowaną liczbą makrofagów (35-40%) oraz niewielką liczbą neutrofili i komórek mezotelialnych (< 5%). Nie zaobserwowano żadnych nietypowych komórek ani czynników etiologicznych. Płyn rozpoznano jako chłonkę.
Dodatkowa diagnostyka obejmowała echokardiogram, który wykazał łagodną niedomykalność zastawki mitralnej i trójdzielnej, ale bez poszerzenia komory oraz zmian grubości ścian serca, i prawidłową kurczliwość. Stwierdzono płyn w jamie opłucnej. Tomografia komputerowa całego ciała (TK) nie dostarczyła żadnych dowodów na obecność nowotworu ani informacji o przyczynie płynu limfatycznego. Limfangiogram TK po podaniu środka cieniującego ujawnił prawidłowe krążenie limfatyczne. Ponieważ przyczyna nie została zidentyfikowana, rozpoznano idiopatyczny płyn w jamie opłucnej.
Możliwości leczenia
Leczenie farmakologiczne
Leczenie farmakologiczne chłonkopiersia obejmuje postępowanie żywieniowe, nakłucie klatki piersiowej w celu usunięcia płynu i/lub stosowanie leków. Usunięcie płynu poprawia komfort pacjenta i powoduje ustępowanie objawów klinicznych, ale rzadko prowadzi do wyleczenia, chociaż istnieje kilka doniesień o spontanicznym ustąpieniu objawów.1,2 Leki stosowane w leczeniu chłonkopiersia obejmują rutynę i/lub analog somatostatyny – oktreotyd. Rutyna jest dodatkiem żywieniowym, który ma zwiększać wychwyt płynu obrzękowego przez naczynia limfatyczne. Jej stosowanie przyniosło pewną poprawę u kotów z chłonkopiersiem, ale nie została ona oceniona u psów.3,4 Oktreotyd – analog somatostatyny, który podawano pozajelitowo psom i kotom z chłonkopiersiem, wykazał niską skuteczność, ponadto jest kosztowny i nie jest szeroko stosowany.1,5,6 W przypadku pacjenta opisanego w niniejszym artykule rozpoczęto podawanie rutyny w dawce 1500 mg doustnie co osiem godzin ze względu na możliwe korzyści. Z uwagi na objawy nudności i braku łaknienia przepisano również lek zobojętniający kwasy, aby wspomóc apetyt (omeprazol 40 mg co 12 godzin przez siedem dni).
Leczenie chirurgiczne
Leczenie chirurgiczne może obejmować podwiązanie przewodu piersiowego, ablację zbiornika chłonnego i/lub perikardiektomię. W przypadku każdej z tych metod odnotowuje się różne wskaźniki skuteczności. Często zabiegi te są łączone dla jej zwiększenia.1 Inną metodą jest umieszczenie portu ułatwiającego drenaż chłonki do przestrzeni otrzewnowej w celu jej wchłonięcia lub do przestrzeni podskórnej w celu jej usunięcia. Rokowanie po leczeniu chirurgicznym waha się od dobrego do doskonałego, ale optymalna metoda chirurgiczna w leczeniu chłonkopiersia u psów nie jest znana ze względu na małą liczbę przypadków i różnorodność zgłaszanych interwencji.