Ograniczanie ryzyka zakaźnych jatrogennych powikłań poprzetoczeniowych u kotów. Wytyczne Europejskiej Rady Ekspertów ds. Chorób Kotów
M.G. Pennisi, K. Hartmann, D.D. Addie, H. Lutz, T. Gruffydd-Jones, C. Boucraut-Baralon, H. Egberink, T. Frymus, M.C. Horzinek, M.J. Hosie, A. Lloret, F. Marsilio, A.D. Radford, E. Thiry, U. Truyen, K. Möstl
Streszczenie
Dzięki lepszej dostępności produktów krwiopochodnych liczba wskazań do przeprowadzania transfuzji u psów i kotów jest coraz większa. Świeża krew pełna również jest łatwo dostępna dla lekarzy weterynarii, ponieważ może zostać pobrana od własnych kotów dawców lub kotów oddających krew jako „honorowi krwiodawcy”. Przetoczenie krwi wiąże się z pewnym ryzykiem dla kota biorcy, gdyż w jego trakcie lub po jego zakończeniu może dojść do wystąpienia ostrych bądź opóźnionych niepożądanych reakcji poprzetoczeniowych o podłożu immunologicznym. Niniejszy artykuł omawia natomiast powikłania spowodowane przez czynniki zakaźne, które mogą przedostać się do krwi biorcy albo poprzez podanie krwi skażonej na skutek jej nieprawidłowego pobrania, przechowywania lub przetoczenia, albo też w wyniku podania krwi od zakażonego dawcy.
Aby zapobiec skażeniu krwi dawcy, należy przestrzegać wieloetapowego schematu postępowania ze strzykawkami i innymi materiałami, ponieważ u kotów krew nie może być pobierana z wykorzystaniem zestawu zamkniętego. Kluczowe znaczenie ma wówczas zachowanie bezwzględnych zasad higieny na każdym etapie. Opakowania na krew muszą być chronione przed przedostaniem się do nich bakterii, gdyż endotoksyny bakteryjne mogą wywołać natychmiastową reakcję gorączkową, a nawet prowadzić do śmiertelnego w skutkach wstrząsu.
Aby zapobiec szerzeniu się chorób zakaźnych drogą krwi, American College of Veterinary Internal Medicine (ACVIM – Amerykańskie Weterynaryjne Stowarzyszenie Chorób Wewnętrznych) przedstawiło podstawowe zasady kwalifikowania dawców krwi pod kątem obecności wybranych zarazków. Według powyższych, akceptowanych na całym świecie kryteriów podstawowy panel badań przesiewowych dla kotów dawców obejmuje wykluczenie u nich zakażenia wirusem białaczki kotów, wirusem niedoboru immunologicznego kotów i Bartonella spp. oraz hemoplazmozy kotów. Lista kryteriów dyskwalifikujących dawcę powinna być dostosowana do sytuacji epidemiologicznej panującej na danym terenie i uwzględniać inne choroby przenoszone przez stawonogi. Najbardziej przydatny, praktyczny, szybki i niedrogi sposób ograniczenia prawdopodobieństwa zakażenia związanego z przetoczeniem krwi polega na ocenie ryzyka ze strony kotów dawców na podstawie pisemnej ankiety wypełnianej przez właściciela zwierzęcia. Niemniej jednak transfuzja krwi nigdy nie powinna być uważana za w pełni bezpieczną.
Wstęp
W ciągu ostatnich kilku lat w medycynie transfuzyjnej małych zwierząt dokonał się znaczący postęp, co przyczyniło się do rozwoju intensywnej terapii i leczenia stanów nagłych. Dostępność produktów krwiopochodnych spowodowała też wzrost liczby wskazań do przeprowadzania transfuzji u psów i kotów, nawet jeśli w niektórych przypadkach medycyna weterynaryjna oparta na dowodach nie potwierdza związanych z nią korzyści (Davidow, 2013).
Świeża krew pełna jest łatwo dostępna dla lekarzy weterynarii, ponieważ może zostać pobrana od własnych kotów dawców lub kotów oddających krew jako „honorowi krwiodawcy”. Ponadto dzięki obecnym na rynku zestawom do określania grup krwi i przeprowadzania prób krzyżowych z wykorzystaniem żelu separującego w warunkach klinicznych, przeznaczonym dla kotów, przetaczanie krwi stało się bezpieczniejsze i bardziej dostępne w praktyce weterynaryjnej (Rudd, 2013a). Niemniej jednak transfuzja krwi wiąże się z ryzykiem dla biorcy oraz w pewnym stopniu również dla dawcy, który zostaje poddany inwazyjnemu zabiegowi wymagającemu sedacji (Spada i wsp., 2014). W tym kontekście należy zawsze dokładnie przeanalizować stosunek ryzyka do potencjalnych korzyści. Powinno się unikać przetaczania krwi pacjentom w terminalnej fazie choroby i rozważyć u nich inne możliwości leczenia (Rudd, 2013b). Co ciekawe, w badaniu przeprowadzonym u ludzi w stanie krytycznym wykazano, że transfuzja krwi nie zmniejsza u nich ryzyka śmierci w ciągu kolejnych 30 dni (Hérbert i wsp., 1999).
W trakcie przetaczania krwi lub po jego zakończeniu, na skutek reakcji immunologicznych, u biorcy może dojść do wystąpienia ostrych bądź opóźnionych niepożądanych reakcji poprzetoczeniowych. Mogą one przyjmować postać od łagodnych stanów gorączkowych* aż po poważne, zagrażające życiu przeciążenie łożyska naczyniowego bądź ostre hemolizy wewnątrznaczyniowe. Omówienie sposobów zapobiegania tego rodzaju reakcjom immunologicznym nie jest celem tego artykułu. Odpowiednie wytyczne Czytelnik może znaleźć w innych źródłach (BSAVA Scientific Committee, 2000; Helm i Knottenbelt, 2010a, 2010b; Barfield i Adamantos, 2011; Davidow, 2013; Rudd, 2013a, 2013b; Kisielewicz, Self, 2014).
Niniejsze zalecenia skupiają się na zapobieganiu przeniesieniu chorób zakaźnych podczas przetaczania krwi u kotów. Niepożądane reakcje wywołane obecnością czynników zakaźnych mogą być spowodowane skażeniem krwi w wyniku jej nieprawidłowego podania, przechowywania bądź przetoczenia albo transfuzją krwi pobranej od zakażonego dawcy.
Zapobieganie skażeniu krwi dawcy
Pobieranie krwi od kotów, w porównaniu z jej pobieraniem u psów, wiąże się z większym ryzykiem skażenia. W przypadku kotów krew nie może bowiem zostać pobrana za pomocą zestawu zamkniętego, tak jak ma to miejsce u ludzi lub u psów, konieczna jest zatem wielokrotna zmiana strzykawek i przyłączanie do nich innych elementów oraz pomoc kilku asystentów. Przekłada się to na większe ryzyko skażenia. Generalnie od kota pobiera się 50 ml krwi za pomocą trzech (20 ml) lub pięciu (10 ml) strzykawek. Każda z nich zawiera odpowiednią ilość antykoagulantu, pobranego z opakowania do pobierania krwi przeznaczonego dla ludzi (Rudd, 2013b). Zazwyczaj igła dożylna połączona jest ze strzykawką łącznikiem typu T i kranikiem trójdrożnym. Strzykawki napełniane są ostrożnie krwią, a następnie obracane w dłoniach przez asystenta. Krew pobrana do strzykawek jest natychmiast wtłaczana przez port wejściowy do pojedynczego opakowania (worka) do pobierania krwi (ryc. 1). Na koniec zostaje przetoczona biorcy za pomocą zestawu wprowadzonego przez inny port opakowania.
Kluczowe znaczenie ma to, aby każdy etap tego zabiegu był przeprowadzany z zachowaniem bezwzględnych zasad higieny, nawet w sytuacji zagrożenia życia pacjenta (FECAVA, 2013). Powierzchnia, na której znajdują się materiały jednorazowego użytku, powinna być jałowa, a personel musi nosić sterylne rękawiczki i maski. Każdą strzykawkę, zarówno po wprowadzeniu do niej antykoagulantu, jak i po nabraniu krwi, trzeba natychmiast zamknąć za pomocą przykrytej igły i nie otwierać aż do chwili przenoszenia jej zawartości do worka na krew. Dobrzuszna okolica szyi dawcy powinna zostać przygotowana jak do zabiegu chirurgicznego. Im więcej czasu upływa od pobrania krwi do przetoczenia, tym większe ryzyko jej skażenia. Pobraną krew należy przechowywać w temperaturze 4°C. Niemniej jednak krew nie powinna być przechowywana po przyłączeniu do zawierającego ją worka zestawu do przetoczenia.
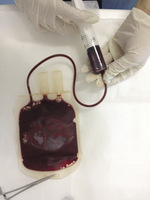
Takich samych zasad należy przestrzegać w przypadku wykonywania autotransfuzji, opisywanej u psów w sytuacjach zagrożenia życia, takich jak krwotok do klatki piersiowej lub jamy brzusznej. Pobiera się wówczas krew z jamy ciała za pomocą wyposażenia umożliwiającego śródoperacyjne odzyskiwanie krwinek, a następnie przetacza je po odpowiednim wypłukaniu** (Tasker, 2013; Kisielewicz i Self, 2014).
Jeżeli do opakowania z krwią przedostaną się bakterie, po jej podaniu u biorcy może wystąpić natychmiastowa reakcja gorączkowa. Jej przyczyną są endotoksyny produkowane przez Gram-ujemne bakterie namnażające się w niskich temperaturach, takie jak Pseudomonas spp., lub bakterie jelitowe, na przykład Serratia marcescens. Ten ostatni mikroorganizm był izolowany z opakowań krwi skażonych bakteriami oraz od kotów, u których po jej przetoczeniu obserwowano gorączkę, wymioty, biegunkę, zażółcenie błon śluzowych, a nawet śmierć (Hohenhaus i wsp., 1997). Najgroźniejszą konsekwencją w tego typu przypadkach jest rozwój wstrząsu prowadzącego do śmierci, wywołanego działaniem endotoksyn.
Opakowania do przechowywania krwi powinno się dokładnie obejrzeć przed użyciem. Jeżeli zaobserwuje się zmianę koloru lub jakąkolwiek inną widoczną zmianę, należy je zniszczyć (Wardrop i wsp., 2005).
Zapobieganie przenoszeniu chorób zakaźnych drogą krwi
Informacje na temat czynników zakaźnych przekazywanych drogą krwi u kotów stają się coraz bardziej powszechne. Dotyczy to szczególnie chorób przenoszonych przez stawonogi (Beugnet i Marié, 2009; Vilhena i wsp., 2013). W 2016 roku American College of Veterinary Internal Medicine (ACVIM) uaktualniło ujednolicone stanowisko przedstawione w roku 2005, odnoszące się do testów przesiewowych w kierunku chorób zakaźnych występujących w krajach Ameryki Północnej, które zaleca się wykonywać u psów i kotów będących dawcami krwi (Wardrop i wsp., 2005; Wardrop i wsp., 2016). Wskazane jest przeprowadzanie badań w kierunku drobnoustrojów, które spełniają co najmniej trzy spośród poniższych kryteriów: 1) udokumentowano przypadki zachorowań u biorców w wyniku przetoczenia krwi, 2) istnieje możliwość zakażenia subklinicznego (nosiciel może nie wykazywać objawów chorobowych), 3) możliwe jest wyhodowanie czynnika chorobotwórczego z krwi zakażonego zwierzęcia, 4) choroba wywoływana przez zarazek ma ciężki przebieg lub jest trudna w leczeniu. Natomiast warunkowe przeprowadzanie badań zaleca się, gdy 1) możliwość przeniesienia drogą krwi udokumentowano jedynie eksperymentalnie lub 2) wywoływana choroba nie ma ciężkiego przebiegu i w większości przypadków organizm jest w stanie łatwo ją zwalczyć.
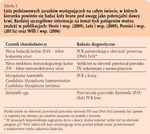
Na podstawie powyższych wytycznych, powszechnie akceptowanych na świecie, panel badań przesiewowych dla kotów dawców (tab. 1) obejmuje wirusa białaczki kotów (FeLV – feline leukaemia virus), wirusa niedoboru immunologicznego kotów (FIV – feline immunodeficiency virus), Bartonella spp. oraz hemoplazmozę kotów (Reine, 2004; Wardrop i wsp., 2005; Gary i wsp., 2006). Jednakże lista drobnoustrojów chorobotwórczych, pod których kątem należy badać koty będące potencjalnymi dawcami krwi, powinna być dostosowana do sytuacji epidemiologicznej na danym obszarze (Hackett i wsp., 2006). Pozostałe zarazki, które można uwzględnić w panelu przesiewowym dla kotów dawców w rejonach endemicznych, przedstawiono w tabeli 2.















