W zależności od lokalizacji wyróżnia się różne postacie chłoniaka:
- chłoniak grasicy/przedniej części śródpiersia
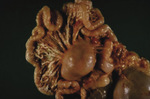
- postać pokarmowa, w której komórki nowotworowe wywodzą się z narządów układu pokarmowego (ryc. 4)
- postać wieloogniskowa lub obwodowa, obejmująca węzły chłonne
- postać atypowa lub pozawęzłowa, w której dochodzi do rozwoju pojedynczych guzów w nerkach, ośrodkowym układzie nerwowym lub skórze.
W niektórych przypadkach chłoniak może mieć postać rozsianą i obejmować wiele różnych narządów i okolic organizmu (Hardy i wsp., 1970; Reinacher i Theilen, 1987). Zajęcie przez chłoniaka wątroby, śledziony, szpiku kostnego, krwi i(lub) narządów nienależących do układu chłonnego wiąże się z gorszym rokowaniem (Vail i Thamm, 2005).
W zależności od tego, jaki rodzaj komórek uległ transformacji nowotworowej, wyróżnia się różne typy białaczek ostrych lub przewlekłych.
U młodych kotów z wiremią sporadycznie opisywano wieloogniskowe włókniakomięsaki, które wiązano z zakażeniem wirusem mięsaka kotów (FeSV – feline sarcoma virus), rozwijającym się z rekombinacji genomu FeLV-A z onkogenami komórkowymi (Hardy, 1981; Donner i wsp., 1982; Besmer, 1983). Włókniakomięsaki wywołane przez wirus FeSV należy różnicować z mięsakami poiniekcyjnymi kotów, które nie mają związku ani z zakażeniem FeLV, ani FeSV.
Inne choroby
U kotów z trwałą wiremią FeLV opisywano łagodne powiększenie obwodowych węzłów chłonnych (Moore i wsp., 1986), którego obraz kliniczny można pomylić z obrazem chłoniaka wieloogniskowego. Wykazywano również zależność pomiędzy postępującym zakażeniem FeLV u kotów, u których wirus był obecny w komórkach krypt jelitowych, a występowaniem przewlekłego zapalenia jelit wywołanego zwyrodnieniem enterocytów oraz martwicą krypt jelitowych (Reinacher, 1987). U kotów z postępującym zakażeniem FeLV opisywano też obecność choroby zapalnej i zwyrodnieniowej wątroby (Reinacher, 1989).
W literaturze opisane są także przypadki zaburzeń neurologicznych niezwiązanych z chłoniakiem OUN bądź z wtórnym zakażeniem tego układu. Większość z nich to neuropatie obwodowe z takimi objawami jak nierówność źrenic (anizokoria), obustronne rozszerzenie źrenic, zespół Hornera, nietrzymanie moczu, nietypowa wokalizacja, przeczulica, niedowłady i porażenia (Haffer i wsp., 1987). Sugeruje to, że wirus FeLV w sposób bezpośredni uszkadza układ nerwowy (Dow i Hoover, 1992).
W przebiegu FeLV opisywano również występowanie chorób na tle immunologicznym, takich jak niedokrwistość hemolityczna, zapalenie kłębuszków nerkowych, zapalenie błony naczyniowej oka oraz zapalenie wielostawowe. Za główne mechanizmy rozwoju tych chorób uznaje się odkładanie się kompleksów antygen–przeciwciało w tkankach oraz utratę czynności limfocytów T-regulatorowych.
Znane są także doniesienia o występowaniu zaburzeń ze strony układu rozrodczego i zespołu słabego kocięcia. Objawiają się one przede wszystkim resorpcją zarodków, ronieniami i śmiertelnością noworodków (Hardy, 1981). Zarówno zespół słabego kocięcia, jak i zaburzenia ze strony układu rozrodczego są obecnie rzadko obserwowane z uwagi na niską prewalencję zakażeń FeLV u kotów rasowych używanych do rozrodu.
Rozpoznawanie
Wykrywanie wolnego antygenu p27 za pomocą testu ELISA
Pierwsze testy immunoenzymatyczne (ELISA) wykrywające antygen p27 opierały się na wykorzystaniu przeciwciał poliklonalnych. Ich niewątpliwą zaletą była możliwość ilościowej oceny antygenu p27. Nierzadko dawały one jednak wyniki fałszywie dodatnie z uwagi na to, że zawarte w nich przeciwciała wykrywały nie tylko białka wirusa, ale sporadycznie wiązały się także z elementami niewirusowymi (Lutz i wsp., 1980b, 1980c).
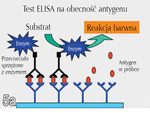
W późniejszych latach wprowadzono nowsze wersje testu ELISA, wykorzystujące przeciwciała monoklonalne skierowane przeciwko antygenowi p27 kapsydu FeLV, które wykrywają to białko we krwi lub w surowicy (ryc. 5) (Lutz i wsp., 1983a, 1983b). Próbkę badanej surowicy miesza się najpierw z jednym bądź dwoma przeciwciałami monoklonalnymi swoistymi dla epitopów B i C białka p27, połączonymi z enzymem, a otrzymaną mieszaninę przenosi się na nośnik (np. płytkę) opłaszczony przeciwciałem monoklonalnym dla epitopu A białka p27. W przypadku obecności w badanej surowicy antygenu p27 zostaje on związany z nośnikiem (wraz z enzymem), co można uwidocznić reakcją barwną wskutek działania enzymu po dodaniu substratu. Obecność białka p27 oznacza wiremię, która, jak wspomniano powyżej, może być trwała (zakażenie postępujące) lub przejściowa (zakażenie regresywne). Zaletą technik ELISA jest wysoka czułość i swoistość w wykrywaniu wiremii.
Wykrycie wolnego antygenu p27 za pomocą immunochromatografii
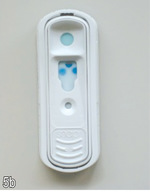
Testy immunochromatograficzne oparte są na tej samej zasadzie co testy ELISA (ryc. 6). W ich przypadku jednak pory złoża rozdzielczego o średnicy mniejszej niż jeden mikron pokryte są raczej przeciwciałami niż enzymami. Wykazano, że czułość i swoistość diagnostyczna testów działających w oparciu o zasadę immunochromatografii jest porównywalna z czułością i swoistością testów ELISA (Robinson i wsp., 1998; Hartmann i wsp., 2001, 2007; Pinches i wsp., 2007; Sand i wsp., 2010; I stopień EBM).